Представьте, что клетки вашего тела – это строительные блоки, из которых возводится сложный организм. Но что, если некоторые из этих блоков вдруг решают стать “кирпичами” жировой ткани, причем в избытке? Именно этот процесс, известный как адипогенез, лежит в основе таких серьезных проблем со здоровьем, как ожирение и диабет 2 типа. До недавнего времени ученые лишь догадывались о механизмах, управляющих этим превращением, но новое исследование корейских ученых проливает свет на этот загадочный путь, открывая потенциальные возможности для будущих терапий.
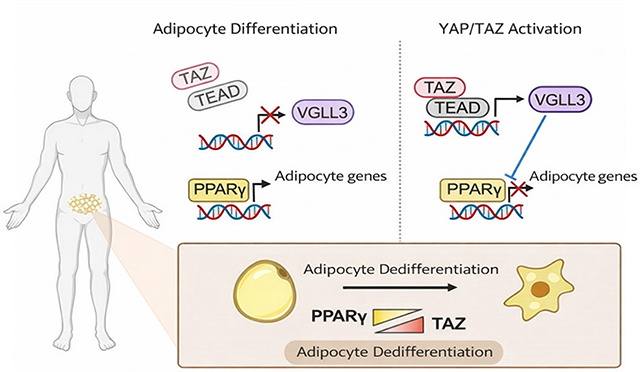
В центре внимания исследователей оказался белок PPARγ, прозванный “главным регулятором” образования жировых клеток. Когда этот белок проявляет активность, он действует как дирижер, запускающий целую симфонию генов, которые неумолимо подталкивают обычную клетку к превращению в адипоцит – зрелую жировую клетку. Задача PPARγ – обеспечить “правильное” формирование и поддержание этой новой идентичности.
Однако, как выяснили ученые из Корейского передового института науки и технологий, этот “дирижер” не действует в вакууме. В ходе детального анализа клеток мышей и самих животных была обнаружена удивительная вещь: инструкции PPARγ на синтез жира могут быть “перехвачены” и заблокированы с помощью специфического эпигенетического “тумблера”. Важно понимать, что эпигенетика – это не изменение самой ДНК, а скорее управление тем, как гены “включаются” или “выключаются”.
Ключевую роль в этом эпигенетическом контроле играют два белка – YAP и TAZ. Они являются частью так называемого сигнального пути Hippo, который, подобно системе автопилота, регулирует рост и развитие наших органов, определяя, должны ли клетки делиться, умирать или “специализироваться” в определенный тип, например, в жировые.
Раньше ученые знали, что YAP и TAZ как-то связаны с образованием жировых клеток, но точный механизм оставался загадкой. Теперь же, сравнивая этот процесс с открытием капота автомобиля для изучения его двигателя, исследователи смогли детально разобраться в этой биологической “машинерии”.
Исследование показало, что YAP и TAZ запускают химическую цепную реакцию, которая эффективно “заглушает” гены, активируемые PPARγ для превращения клетки в жировую. Таким образом, даже если PPARγ пытается “приказать” клетке стать жировой, YAP и TAZ могут игнорировать эту команду, сохраняя клетку в более “незрелом”, пластичном состоянии.
В норме активность YAP и TAZ жестко контролируется сигнальным путем Hippo, который действует как своего рода “тормоза”. Но что произойдет, если эти “тормоза” снять? Ученые провели эксперимент, отключив сигнальный путь Hippo у мышей. Результат оказался впечатляющим: YAP и TAZ стали гиперактивными, а существующие жировые клетки начали “отступать” от своего специализированого состояния.
Эти клетки не вернулись полностью к состоянию стволовых, но они утратили многие из своих характерных признаков и стали вести себя скорее как клетки-предшественники – более универсальные и способные потенциально трансформироваться в другие типы клеток.
Эти открытия открывают гораздо более ясное понимание того, как мы можем управлять балансом жировых клеток в организме – увеличивать или уменьшать их количество. Хотя эти эксперименты пока проводились только на мышах, их результаты дают надежду на разработку новых терапевтических стратегий.
Избыток жира в организме или его накопление в нежелательных местах – это прямая дорога к целому ряду проблем со здоровьем. А когда жировые клетки уже сформировались, от них крайне сложно избавиться. При похудении они обычно сжимаются, но не исчезают полностью.
Понимание того, как регулируется превращение клеток в жировые, может однажды привести к созданию новых способов лечения метаболических заболеваний. Вместо общих подходов, мы сможем более точно нацеливаться на накопление жира, хотя путь к безопасным и эффективным методам, безусловно, потребует дальнейших масштабных исследований.
“Это исследование заложило важную основу для более глубокого понимания механизмов, лежащих в основе изменений идентичности жировых клеток, и, в долгосрочной перспективе, для разработки персонализированных стратегий лечения пациентов с метаболическими заболеваниями”, – заключает молекулярный биолог Дэ-Сик Лим, один из ведущих авторов исследования.
Результаты исследования опубликованы в журнале Science Advances.
Изображение: Корейский передовой институт науки и технологий