Ученые Института биофизики будущего МФТИ с коллегами предложили альтернативу лечению нарушений ритма сердца с помощью приборов-кардиостимуляторов. Это биоинженерные конструкции из клеток, управляемые светом с помощью белка канального родопсина-2. Исследователи проверили свой биологический стимулятор на реальном сердце крысы, сделав первый шаг на пути его использования в клинике. Работа выполнена при поддержке Российского научного фонда (грант №25-65-00037) и опубликована в журнале «Патология кровообращения и кардиохирургия».
Нарушения сердечного ритма, такие как дисфункция главного ритмоводителя сердца (синусового узла) и атриовентрикулярная блокада (когда электрический стимул хуже проходит от предсердий к желудочкам) остаются одной из самых серьезных и опасных проблем со здоровьем. По сути, это критические сбои в «электропроводке» сердца, которые мешают ему нормально сокращаться, качать кровь и потому представляют угрозу для жизни.
Самым надежным методом лечения таких нарушений сердечного ритма считается установка искусственного электрокардиостимулятора (ЭКС). Это устройство — настоящий технологический прорыв своего времени, который спас миллионы жизней. И все же ЭКС имеет недостатки и далек от совершенства. Развитие современных технологий кардиостимуляции призвано сделать лечение более щадящим и избавить пациентов от проблем и рисков (тяжелые хирургические операции, обслуживание прибора-кардиостимулятора, опасность его отказа и т. д.).
Одно из самых перспективных направлений — создание крошечных биорезорбируемых приборов, которые со временем сами «растворяются» в организме и используются для временной кардиостимуляции. Например, ученые уже научились использовать свет для управления ритмом сердца: специальные кремниевые частицы, внедренные в ткани, в ответ на световые лучи генерируют электрические сигналы. Другой вариант — миниатюрные устройства размером около двух миллиметров, которые заряжают с помощью беспроводной технологии. Они полностью исчезают, когда сердце пациента восстанавливается и начинает нормально работать. Это особенно удобно и безопасно, так как кардиостимулятор не нужно удалять с помощью повторной хирургической процедуры.
Тем не менее даже у таких технических новинок пока есть свои минусы. Из-за того что они постепенно растворяются, они работают недолго и могут подавать стимулы нестабильно. Кроме того, используемая в них беспроводная передача энергии может давать сбои при движении человека или из-за внешних помех, а сама технология остается очень дорогой и все еще требует длительных клинических испытаний.
Поэтому ученые лаборатории экспериментальной и клеточной медицины Института биофизики будущего МФТИ и их коллеги из клинических центров Москвы и Новосибирска, объединив все лучшие наработки, создали новую технологию — гибридный оптический кардиостимулятор. Идея заключается в том, чтобы использовать модифицированные клетки прямо внутри сердца для выращивания новой ткани, которая станет полноценной функциональной частью органа. Для управления такой тканью применяется оптогенетика — метод, позволяющий контролировать работу клеток с помощью света. Он использует особые светочувствительные белки (вроде родопсина человеческого глаза), которые способны переключаться из одного состояния в другое под действием лучей с определенной длиной волны. Такие белки-выключатели при активации меняют свойства мембраны клетки, в которой находятся. Могут возбуждать ее или, напротив, «успокаивать», либо вызывать другую реакцию.
Поскольку стимулятор состоит из живых клеток, он может расти вместе с организмом пациента и работать максимально естественно. В то же время врачи сохраняют возможность четко настраивать сердечный ритм извне с помощью световых сигналов.
В рамках новой работы такой светочувствительный кардиостимулятор испытали на изолированном работающем сердце лабораторных крыс. В ходе эксперимента использовали клетки, полученные из сердца новорожденных крысят, а также человеческие кардиомиоциты, выращенные в лаборатории из стволовых клеток. Чтобы они начали реагировать на свет, в клетки ввели ген, который кодирует реагирующий на свет белок — канальный родопсин-2. Так клетки приобрели свойство контролируемо сокращаться, вырабатывая электрический импульс каждый раз, когда на них направляли синий свет. Затем эти модифицированные клетки поместили на полимерные носители — подложки, которые помогают клеткам лучше прижиться и закрепиться в организме. Получившуюся конструкцию проверили на работающем сердце крысы, используя засветку синим светом для контроля сокращений подсаженных клеток.
Сразу после подсадки клеток на поверхность сердца проверили, как взаимодействуют сердце и новая «заплатка» на нем. Поначалу они работали несинхронно: сердце билось в своем собственном ритме, а патч (встроенная часть ткани) — в другом. Под действием синего света имплантат контролируемо сокращался, а само сердце на это никак не реагировало и не меняло ритм. Выходит, исходно между сердцем и новой тканью еще не наладилась связь, поэтому они не могли работать как единое целое.
Однако спустя некоторое время ситуация изменилась: между вживленными клетками и тканью самого сердца началось взаимодействие, что позволило управлять сокращением всего органа с помощью света. Новые фоточувствительные клетки успешно прижились и начали работать как настоящий биологический светоуправляемый кардиостимулятор.
«Нашей целью было создание гибридного биологического кардиостимулятора, управляемого светом. Основная идея — объединение клеточной терапии и оптогенетики. Наш эксперимент показал, как такие клетки встраивались на поверхность изолированного крысиного сердца: фотостимуляция задавала частоту сокращений, подтверждая возможность использования клеток как водителей ритма в дальнейшем. Мы увидели, что такой фотоуправляемый пейсмейкер способен устанавливать функциональный контакт с миокардом примерно через 35 минут и задавать сердечный ритм в ответ на световую стимуляцию клеток»,— отметила Елена Турчанинова, младший научный сотрудник лаборатории экспериментальной и клеточной медицины Института биофизики будущего МФТИ.
В работе кроме сотрудников Института биофизики будущего МФТИ принимали участие их коллеги из Национального медицинского исследовательского центра им. Е.Н. Мешалкина и Московского областного научно-исследовательского клинического института им. М.Ф. Владимирского.
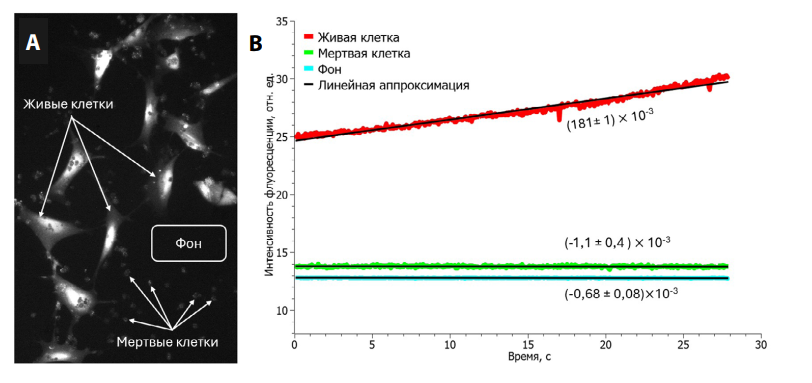
Изображение на обложке: оптогенетическая модификация кардиомиоцитов человека, дифференцированных из ИПСК: А – оптическое картирование культуры при фотостимуляции; B – динамика кальциевой флуоресценции в живых клетках, мертвых клетках и фоне с линейной аппроксимацией. Источник: «Патология кровообращения и кардиохирургия»
Источник: Центр научной коммуникации МФТИ