Ученые разработали биосовместимый гидрогель, который можно использовать для заполнения полостей в мозге после удаления опухолей, а также для доставки лекарств. Гидрогель высвобождает противоопухолевые препараты, тем самым предотвращая повторное возникновение новообразования. При этом материал безопасен для здоровых клеток - он снижает их жизнеспособность не более чем на 25%, тогда как обычная химиотерапия часто оказывается более токсична.
Результаты исследования, поддержанного грантом Президентской программы Российского научного фонда (РНФ), опубликованы в журнале Carbohydrate Polymers.
Глиобластома - это наиболее агрессивная форма рака головного мозга. Ее лечат, сначала удаляя опухоль хирургически, а затем проводят лучевую и химиотерапию. Несмотря на такой подход, выживаемость пациентов за последующие пять лет составляет 6%. Более того, при хирургическом удалении опухоли в 90% случаев она возникает снова вблизи первичного очага. Поэтому нужны препараты, которые бы предотвратили рецидив: доставлялись прямо в послеоперационную полость и обеспечивали длительное действие.
На сегодняшний день существует только одна коммерческая система для доставки противоопухолевого лекарства в послеоперационные полости - разработанная в Японии пластина из биоразлагаемого полимера. Однако ее использование затрудняется тем, что она не может повторить анатомию полости, поэтому ученые ищут альтернативные материалы.
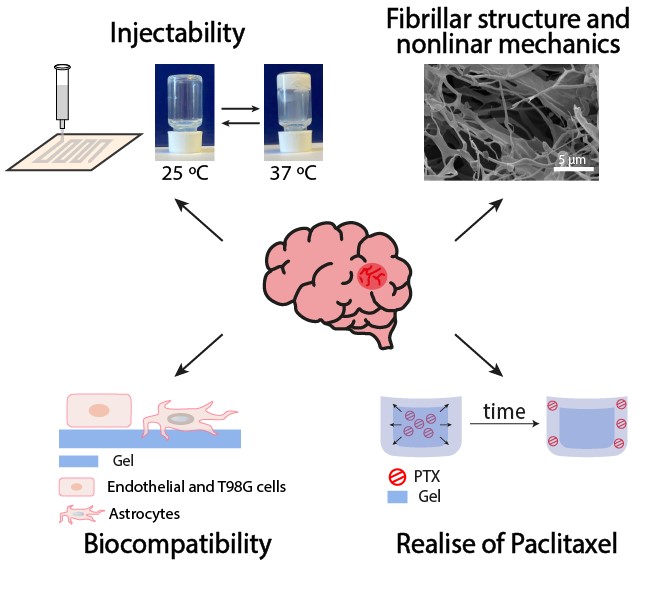
Так, исследователи Московского государственного технического университета имени Н.Э. Баумана с коллегами предложили доставлять противоопухолевые препараты в ткани головного мозга с помощью мягкого биосовместимого термочувствительного материала - гидрогеля. Ученые разработали его на основе коммерчески доступных соединений - нанокристаллической целлюлозы и поли(N-изопропилакриламида) - полимера, водные растворы которого при нагревании переходят из набухшего состояния в "сжатое" (гидрофобное), теряя около 90% объема.
При нагревании до температуры человеческого тела (37°С) модифицированные полимером наночастицы целлюлозы превращались в гель, то есть становились более плотными. Концентрацию частиц можно выбирать таким образом, чтобы конечный материал максимально соответствовал механическим свойствами нужной области мозга.
При нагревании до температуры человеческого тела (37°С) модифицированные полимером наночастицы целлюлозы превращались в гель, то есть становились более плотными. Концентрацию частиц можно выбирать таким образом, чтобы конечный материал максимально соответствовал механическим свойствами нужной области мозга.
- Анастасия Беляева, первый автор статьи, аспирант, инженер Научно-образовательного центра "Мягкая материя и физика флюидов" МГТУ имени Н.Э. Баумана
- Анастасия Беляева, первый автор статьи, аспирант, инженер Научно-образовательного центра "Мягкая материя и физика флюидов" МГТУ имени Н.Э. Баумана
Специалисты протестировали гидрогель на эндотелиальных (выстилающих стенки кровеносных сосудов) и астроглиальных (составляющих основу нервной ткани) клетках, которые выделили из коры головного мозга крыс. Клетки нанесли на слой гидрогеля, а затем наблюдали, как они растут и делятся. Оба типа клеток прилипли к гелю и стали разрастаться. Однако исследователи зафиксировали, что на третьи сутки клетки стали на 25% менее жизнеспособными по сравнению с
клетками, выращенными в стандартном растворе. Тем не менее, полученные данные о жизнеспособности клеток находились в пределах нормы.
Затем авторы "загрузили" в полученный гидрогель противоопухолевое лекарство паклитаксел и нанесли этот состав на клетки глиобластомы человека. Паклитаксел выбрали как одно из эффективных средств против различных опухолей, в том числе глиомы и глиобластомы. Введение противоопухолевого препарата позволило снизить выживаемость раковых клеток с 75% (при
использовании чистого гидрогеля) до 25%.
При доставке в мозг лекарство должно высвобождаться постепенно. Вначале концентрация высвободившегося препарата будет ниже, чем при его использовании в чистом виде, без носителя, но затем она будет нарастать с течением времени, достигая необходимой терапевтической дозы. Таким образом, гель с паклитакселом можно вводить в более высокой дозировке, формируя депо препарата, которое позволит обеспечить необходимый длительный лечебный эффект и при этом не будет блокировать деление здоровых клеток.
Авторы подчеркивают, что полученный материал открывает новый подход к комбинированному лечению онкологических заболеваний головного мозга. Он включает хирургическое удаление опухоли и последующее заполнение послеоперационной полости гидрогелем, содержащим химиотерапевтический препарат. Несомненным достоинством разработанной системы доставки будет возможность заполнять полости любой формы, а также локальный характер химиотерапевтического лечения, снижающий риск побочных эффектов.
В дальнейшем мы планируем глубже изучить биосовместимость геля с тканями головного мозга и протестировать большее количество лекарств разного типа для анализа применимости системы.
- Софья Морозова, кандидат химических наук, старший научный сотрудник Научно-образовательного центра "Мягкая материя и физика флюидов" МГТУ имени Н.Э. Баумана, заведующий лабораторией технологий ионообменных мембран Московского физико-технического института.
В исследовании также принимали участие сотрудники Института физиологически активных веществ РАН (Москва), Института высокомолекулярных соединений РАН (Санкт-Петербург), Института цитологии РАН (Санкт-Петербург), Санкт-Петербургского государственного университета (Санкт-Петербург), Научного центра неврологии (Москва) и Московского физико-технического института (Москва).
Изображение на обложке: пресс-служба РНФ