Графит представляет собой достаточно простой природный минерал, состоящий всего из одного химического элемента, — углерода. Однако кристаллическая слоистая структура придает материалу необычные свойства в виде огнеупорности и электропроводности, благодаря которым он часто используется в промышленности, металлургии, медицине и электротехнике.
Сегодня мы поговорим о том, как устроен графит, об особенностях его добычи и переработки. Кроме того, вы узнаете о природных условиях формирования графита, о том, как люди научились синтезировать этот минерал и нашли области для его практического применения.
Что такое графит?
Графит — это одна из кристаллических форм углерода, которая образуется в недрах Земли в условиях высокой температуры и давления. Когда эти показатели продолжают повышаться, из графита формируется алмаз, который также является аллотропной модификацией углерода. Минерал имеет темный цвет с различными оттенками черного, серого и синего. Название «графит» происходит от древнегреческого «графо» (γράφω), что в переводе на русский язык означает «записывать». Это связано с тем, что материал очень мягок и легко расслаивается, поэтому его используют для производства карандашных стержней.

Структура графита: как устроен материал
Графит, в отличие от многих других веществ, состоит не из молекул, а из слоистых атомных структур. При образовании графита формируются ячейки из 6 атомов, которые имеют форму гексагона (правильного шестиугольника). В природе данная форма является одним из лучших способов организации пространства — такую же структуру имеют, например, пчелиные соты. Внутри каждого слоя атомы достаточно крепко связаны друг с другом, однако между слоями связь уже не так прочна, чем и объясняется мягкость графита.
В зависимости от особенностей структуры выделяют 2 модификации минерала:
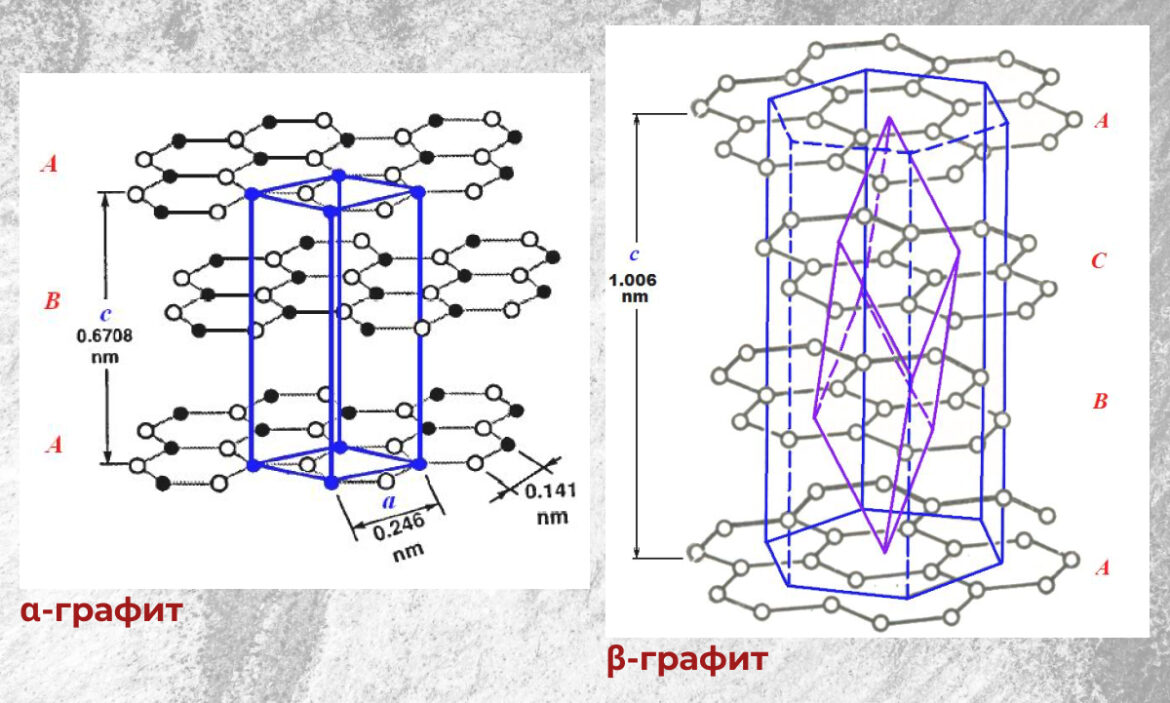
- α-графит (гексагональный) — атомы, формирующие слой, расположены по центру шестиугольников в соседних слоях. Иными словами, слои чередуются через один;
- β-графит (ромбоэдрический) — шестиугольники располагаются с небольшим смещением. В результате атомы каждого первого слоя находятся строго под атомами каждого четвертого. β-графит нельзя добыть в чистом виде, так как он является промежуточной формой α-графита.
Физические и химические свойства графита
Слоистая структура графита обеспечивает ему высокую электропроводность, но только в направлении, параллельном плоскости слоев. При обычной температуре графит проводит электрический ток хуже большинства металлов, превосходя лишь чугун, ртуть и некоторые железные сплавы. Однако при нагревании до температуры 2 200 °C происходит рекристаллизация вещества, то есть изменение структуры за счет образования новых ячеек. В таком состоянии удельное сопротивление материала (обратная величина электропроводности) достигает своего минимального значения — 0,0075 Ом * мм2/м.
Не менее важными физическими свойствами графита являются огнеупорность и термостойкость. Отметим, что в свободной форме углерод имеет весьма низкую температуру воспламенения — около 300 °C в кислородной среде (столько же, сколько у дерева). Однако при формировании кристаллической решетки этот показатель увеличивается более чем в 2 раза. Чтобы поджечь графит, его необходимо разогреть до 700 °C. В естественных условиях графит не плавится — для этого необходимо достичь температуры около 4 000 °C и давления в несколько миллиардов паскалей.
Среди химических свойств графита можно отметить его высокую инертность — материал не растворяется в водной, щелочной и кислотной среде. Чтобы растворить минерал, его необходимо поместить в расплавленный металл. Подойдут железо, платина, никель, хром и другие металлы с высокой температурой плавления. При этом графит образует соединения с щелочными металлами, галогенами и солями, находя благодаря этому применение в химическом машиностроении и топливной энергетике.
Типы графита: природный, синтетический и биографит
Природный графит встречается в месторождениях различных пород, минералов и полезных ископаемых: каменного угля, кварца, мрамора, сланцев и др. В зависимости от условий залегания выделяют 3 разновидности натурального графита.
- Жильный — крупные и плотные кристаллы.
- Чешуйчатый — средние по размеру и плотности кристаллы.
- Аморфный — мельчайшие кристаллы с наименее низкой плотностью.
Графит образуется не сам по себе, а лишь в процессе метаморфизма (структурного изменения материалов). Для этого необходим углерод из других осадочных пород, которые подвергаются воздействию высокой температуры и давления. Подробнее об условиях формирования природного графита мы поговорим в следующем разделе.
Помимо природного, существует и синтетический графит. Как и многие другие синтетические вещества, он был получен случайно. В 1896 году американский химик Эдвард Гудрич Ачесон проводил лабораторные эксперименты с открытым им же карбидом кремния (неорганическим соединением кремния с углеродом). Ученый обнаружил, что при нагревании до температуры 4 150 °C кремний полностью испарился, а остался лишь кристаллический углерод — графит. Сегодня минерал синтезируют путем переработки нефтепродуктов или природного графита.
Биографит — это достаточно редкий вид графита, который создают из экологически чистых материалов с целью снижения выбросов парниковых газов. Сырьем для его изготовления служат побочные продукты лесозаготовки — древесная щепа. Нагревая древесину в герметичной емкости, из нее получают уголь. Затем в лабораторных условиях из угля получают биографит, который не уступает по качеству синтетическому графиту. Эта технология запатентована новозеландской компанией CarbonScape, которая поставляет материал производителям литий-ионных аккумуляторов.

Условия формирования графита в природе
В большинстве случаев графит образуется на границах взаимодействия литосферных плит. Для его формирования необходимо давление 517 мегапаскалей и температура 750 °C. В таких условиях запускается метаморфизм содержащих углерод осадочных и магматических пород. В результате этого процесса формируется графит и сопутствующие ему минералы. Для сравнения добавим, что для формирования алмазов температура должна достигнуть 1 300 °C, а давление — 6 гигапаскалей.
Для производства электрических устройств подходит графит, образованный посредством гидротермального метаморфизма. Разогревающиеся под высоким давлением водные растворы циркулируют по трещинам и порам в горных породах, изменяя их свойства. Гидротермальный графит редко встречается в природе, однако имеет очень прочную кристаллическую структуру.
Некоторое количество графита попало на Землю во время активной бомбардировки метеоритами. Исследования найденных образцов показали, что они сформировались раньше, чем Солнечная система (около 4,5 млрд лет назад). Это указывает на то, что минерал может формироваться в молекулярных туманностях, образованных в результате взрывов сверхновых звезд.
Добыча графита
Природный графит добывают 2 основными способами.
- Открытый. Когда минерал располагается близко к поверхности, его добывают с помощью разработки карьеров (взрывов и бурения). Таким способом можно добыть только чешуйчатый или аморфный гранит.
- Подземный. При глубоком залегании графита разработка карьеров неэффективна, поэтому для добычи используют шахты, глубина которых варьируется от 30 до 80 метров. Используя данный метод, можно добывать жильный графит, имеющий наиболее высокую плотность.

Абсолютным мировым лидером по добыче графита является Китай, который ежегодно производит порядка 800 000 тонн природного графита (примерно 50% от общемирового объема). Крупные месторождения графита также разрабатываются в Индии, Бразилии, Турции и Корее. В России в последние годы добывается от 12 000 до 15 000 тонн графита — приблизительно 1% от мировой добычи.
Переработка графита
На первом этапе переработки графит дробят на мелкие куски, а затем обогащают, то есть удаляют всевозможные примеси. Обогащенный графит отправляют для дальнейшей переработки.
Для получения синтетического графита с различными характеристиками (разные марки графита) используют различные методы переработки. Чаще всего их порядок выглядит следующим образом:
- измельчение;
- обогащение;
- очистка;
- формирование углеродной массы;
- прессование заготовок;
- термическая обработка.
Применение графита
Как уже было упомянуто, переработка позволяет получать разные марки графита. Мы рассмотрим наиболее популярные из них и определим область их практического применения.
- Крупнозернистый (ЭГ) — такой графит используют в производстве электродов для литий-ионных аккумуляторов с низким сопротивлением и повышенной прочностью. Также он подходит для изготовления защитных экранов, нагревателей и стержней для осаждения воды.

- Среднезернистый (3ОПГ, ГМ3) — имеет более плотную структуру по сравнению с электродным графитом и почти не содержит примесей. Его используют для создания промышленного оборудования, насыщения металлов углеродом и производства защитных блоков для научных и медицинских приборов, предназначенных для работы в агрессивной среде.
- Мелкозернистый (МГ, МПГ) — наиболее плотная и очищенная разновидность графита. За счет повышенной прочности он подходит для изготовления литейных и пресс-форм, преобразователей электрического тока (выпрямителей), вакуумных печей и сложной химической аппаратуры.
Вопрос-ответ
Что за материал графит?
Графит — это углеродный кристаллический минерал, который образуется естественным образом в литосфере и синтезируется с помощью вспомогательных материалов.
Из чего состоит графит?
Графит состоит из углерода, атомы которого располагаются особым образом, формируя шестиугольные ячейки.
Чем отличается графит от графена?
Графит является слоистым материалом. Его изолированный слой толщиной всего в один атом называют графеном. Слой графена в 200 раз превосходит по прочности слой стали такой же толщины.
Чем опасен графит?
Пыль и пары графита представляют опасность при их высокой концентрации, например, в местах добычи или лабораториях. При контакте с большими дозами графита происходит раздражение кожи, дыхательных путей и слизистых оболочек.
Где применяют графит?
Графит применяют в электротехнике, химической и тяжелой промышленности, металлургии, медицине и при производстве карандашей.
Изображение на обложке: Freepik








