Фосфор — это крайне необходимый человеку макроэлемент. Его история началась со странных алхимических опытов, но и в последующем он не раз удивлял своими свойствами химиков и биологов. В нашем организме фосфор выполняет важнейшие структурные и энергетические функции, и на его долю приходится 1% от всей массы тела человека. В этой статье мы подробно познакомимся с химическими особенностями и биологической ролью фосфора, узнаем, сколько этого макроэлемента нужно потреблять каждый день, а также рассмотрим характерные признаки дефицита и избытка фосфора.
История открытия и изучения фосфора (P)
Фосфор является первым в истории химическим элементом, первооткрыватель которого точно известен. Немецкий алхимик XVII века Хенниг Бранд был одним из многих экспериментаторов, увлеченных идеей поиска философского камня — мифической материи, способной дарить бессмертие и превращать любые металлы в золото. По его убеждению, ключом к созданию камня должна была стать «жизненная сила», которую можно извлечь из биологических жидкостей. Бранд пришел к весьма пикантному выводу о том, что основой таинственной материи должна быть моча, так как она имеет схожий с золотом цвет.
В 1669 году он собрал колоссальные объемы жидкости (прим. ред.: различные источники упоминают о сотнях и даже тысячах литров) и проводил с ней множество экспериментов, смешивая с другими веществами и варьируя параметры среды. В одном из опытов Бранд выпарил мочу до состояния густого сиропа и поместил этот вываренный субстрат в реторту — герметичный сосуд для перегонки. Раскалив реторту докрасна и достигнув температуры порядка 1 000 °C, он по окончании опыта обнаружил на дне вместо золота белое жидкое вещество, которое на воздухе вспыхнуло огнем. После этого Бранд незамедлительно накрыл его прозрачной банкой и заметил, что субстанция затвердела и начала излучать бледное зеленоватое свечение.
Современные ученые понимают, что Бранд случайным образом воспроизвел реакцию восстановления, однако сам он был убежден в мистической природе полученного вещества. Алхимик назвал его «фосфором» (прим. ред.: от древнегреческого «φωσφόρος» — «несущий свет») и долго хранил рецепт его получения в секрете, но затем все же продал, открыв информацию для научного сообщества.
В первой половине XVIII века фосфор использовали как элемент «магических» шоу и даже пытались лечить им болезни, что зачастую заканчивалось плачевно. Как выяснилось в будущем, белый фосфор представляет собой смертельно опасный яд.
Наконец, в 1769 году шведский химик Юхан Ган совершил прорывное открытие, обнаружив, что фосфор содержится в костях животных. Совместно со своим другом и коллегой Карлом Вильгельмом Шееле он разработал более эстетически приятный метод производства фосфора, включавший обработку костной золы серной кислотой с последующим смешиванием с углем и дистилляцией. После открытия Гана и Шееле легковоспламеняющийся фосфор начали использовать для производства спичек.

В 1840 году немецкий химик Юстус фон Либих открыл критическую значимость фосфора для роста растений. После этого им сильно заинтересовались предприимчивые ученые, которые один за другим патентовали методы производства удобрений на основе фосфора и калийных солей. Открытие фосфатных руд в 1850-х годах дало заметный стимул к развитию всей сельскохозяйственной отрасли. Также повышенный интерес к фосфору проявляли биологи. Обнаруживая его в самых разных частях организма, они шаг за шагом расширяли познания о значимости фосфора для жизни.
Химические свойства и особенности фосфора
Фосфор — это химически активный неметалл с атомным номером 15 и обозначением P. В природной среде, как и в организме человека, он не встречается в чистом виде, так как быстро образует соединения с кислородом и металлами. Однако существуют способы получать чистый фосфор, причем в разных аллотропных модификациях (прим. ред.: формах, имеющих одинаковый химический состав, но отличающихся по структуре). Поговорим о 3 основных аллотропах фосфора.
- Белый фосфор — историческая форма, визуально похожая на воск и обладающая сильнейшим токсическим воздействием. В ее структуре атомы фосфора соединяются в тетраэдры и имеют крайне нестабильные связи. Из-за высокой реакционной способности вещество окисляется, нагревает само себя и воспламеняется при температуре 34 °C. Свечение фосфора или, как его называют химики, хемилюминесценция, также является следствием окисления. При небольшом притоке воздуха образуются окисленные частицы, которые переходят из возбужденного состояния в стабильное, испуская энергию в виде фотонов.
- Красный фосфор — стабильная и менее токсичная модификация, которую получают путем нагрева белого фосфора в безвоздушной среде. В результате трансформации атомы фосфора уже не образуют отдельных молекул, а соединяются в очень длинные цепочки с прочными связями — полимеры. Красный фосфор воспламеняется при температуре от 240 °C. Именно он входит в состав боковой панели спичечного коробка. Энергия трения разрушает химические связи в полимере, из-за чего образуется мизерное количество белого фосфора, который воспламеняется и запускает цепную реакцию в головке спички.
- Черный фосфор — самая термически устойчивая и химически инертная форма. Получать его сложнее, чем другие аллотропы. Для этого необходимо достигнуть давления в 12 000 атмосфер при температуре 200 °C. В результате атомы фосфора выстраиваются в слоистую кристаллическую решетку. Похожее строение имеет графит, но в его структуре выделяются плоские слои, а в структуре черного фосфора — складчатые. Материал проводит электрический ток, а точнее, является полупроводником, благодаря чему рассматривается как перспективный компонент для высоких технологий.

Биологическая роль и функции фосфора в организме
Если бы в организме человека содержался чистый фосфор, мы буквально сгорали бы изнутри из-за его химической активности. Вместо этого он всегда находится в окисленной форме, образуя фосфатную группу PO4. Фосфатные группы выступают в роли «строительных блоков» фосфатов — жизненно важных соединений, которые можно разделить на 2 основные категории.
- Неорганические фосфаты (соли) — фосфатные группы соединяются с металлами, в том числе кальцием, калием, натрием и магнием. Больше всего подобных соединений сосредоточено в твердых тканях, костях и зубах, в виде биологического минерала гидроксиапатита (Ca5(PO4)3OH), обеспечивающего механическую жесткость скелета. Незначительное количество неорганического фосфора находится в растворенном виде в крови, внутри клеток, мягких тканей и органов.
- Органические фосфаты (эфиры) — фосфатные группы соединены с биологическими молекулами, среди которых белки, жиры, углеводы, ферменты и нуклеиновые кислоты ДНК и РНК. Находясь в тесной связи с углеродной основой молекул, фосфатные группы инициируют различные реакции, связанные с выплеском энергии, изменением формы и активности веществ, влиянием на растворимость и многими другими трансформациями.
Фосфор и здоровье костей, зубов и суставов
Примерно 80% всего фосфора в организме человека сосредоточено в костях, в составе ранее упомянутого минерала гидроксиапатита. Его микроскопические кристаллы заполняют собой пространство между волокнами эластичного коллагена, благодаря чему кости становится не только гибкими, но и прочными. Кроме того, костная ткань — это очень динамичная структура, которая постоянно обновляется в течение жизни. После того как старая ткань разрушается, специальные клетки — остеобласты — создают на ее месте мягкий белковый слой. Фосфор отвечает за его минерализацию, то есть укрепление костей в процессе обновления. Этот процесс имеет важное значение и для здоровья суставов, которым для поддержания правильной геометрии необходимо опираться на крепкие кости.
Зубная эмаль, которая является самой твердой тканью в организме человека, практически полностью состоит из гидроксиапатита. Фосфор вместе с кальцием постоянно восстанавливают эмаль, нивелируя воздействие сахаров и кислот из пищи и предотвращая кариес. Также фосфор входит в состав дентина — ткани зубов, расположенной непосредственно под эмалью. В ней макроэлемент отвечает за придание плотности, необходимой, чтобы зуб не трескался во время пережевывания. Также дентин уплотняет стенки вокруг зубных канальцев — если фосфора в организме не хватает, дентин становится пористым, и горячая или холодная пища начинают раздражать нервы.
Фосфор и энергетический обмен организма
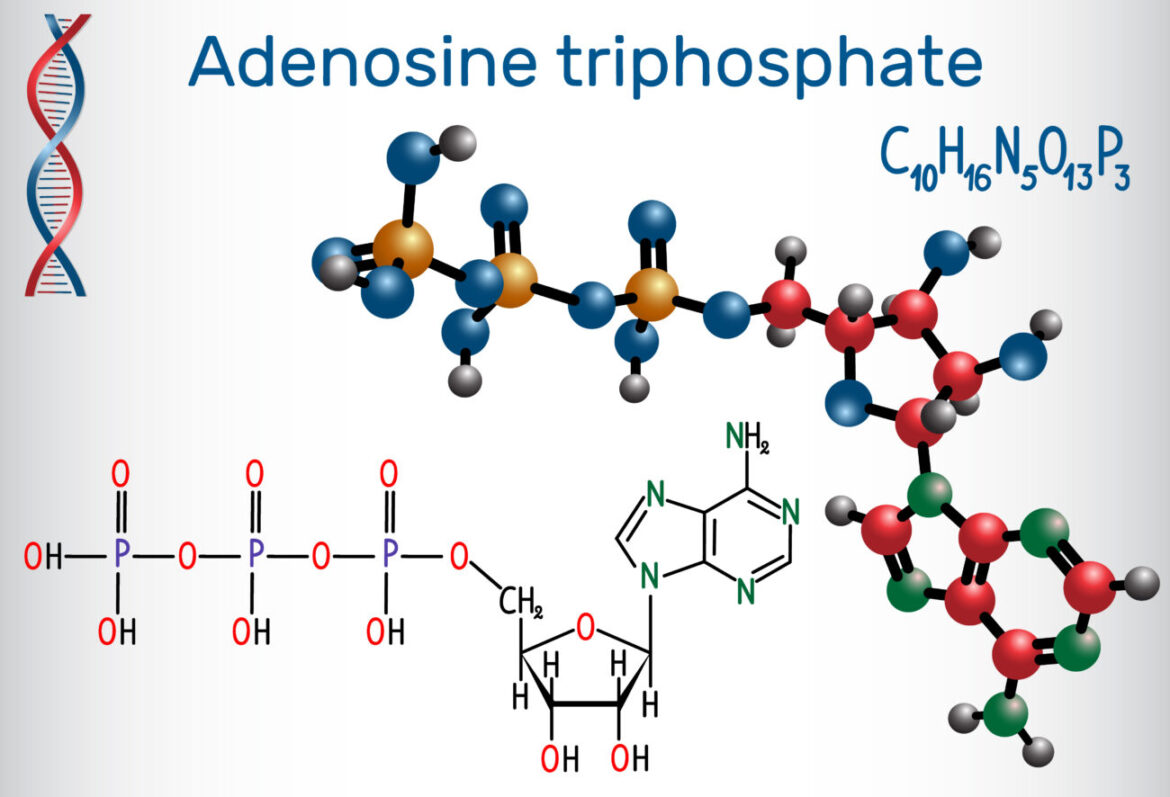
Главной энергетической единицей в нашем организме является аденозинтрифосфат (АТФ) — углеводная молекула с азотистым основанием, к которой присоединены сразу 3 фосфатные группы. Связи между этими группами называют макроэргическими. Это означает, что они обладают колоссальной потенциальной энергией. Когда клетка испытывает энергетическую потребность, она забирает одну фосфатную группу у АТФ, преобразуя его в аденозиндифосфат (АДФ). Разрыв связей сопровождается выплеском энергии, которую клетка тут же использует для своих целей. Организм постоянно «перезаряжает» АДФ, извлекая новые фосфатные группы из пищи.
Кроме того, у нашего организма есть резервный источник энергии, который можно использовать в критический момент. Им является креатинфосфат — естественная азотсодержащая кислота креатин с присоединенной фосфатной группой. Когда мы испытываем интенсивные нагрузки, например, занимаемся спортом или физически тяжелой работой, запасы АТФ быстро истощаются. Тогда при посредничестве фермента креатинкиназы креатинфосфат моментально отдает свою фосфатную группу «разряженной» молекуле, и мышцы снова получают возможность потреблять энергию.
Фосфор и соединение нуклеиновых кислот
Молекулы ДНК и РНК представляют собой длинные полимерные цепи, состоящие из отдельных звеньев органических соединений — нуклеотидов. Важной структурной частью нуклеотида является фосфатная группа, отвечающая за скрепление сахаров — дезоксирибозы и рибозы. Таким образом, фосфор напрямую влияет на геометрическую стабильность молекул, составляющих саму основу жизни. Кроме того, отрицательно заряженные фосфатные группы делают ДНК растворимой в воде, чтобы она могла находиться в среде клеточного ядра, а также участвуют в репликации ДНК — создании новых молекул.
Основные источники фосфора в продуктах питания
Фосфор содержится во многих продуктах как животного, так и растительного происхождения, однако организм значительно лучше усваивает его из животной пищи (прим.ред.: по усредненным данным, 60% против 45%). Это связано с тем, что в растениях фосфор связан с фитиновой кислотой, а у человека попросту нет фермента для ее полного расщепления. Также важно учитывать, что термическая обработка продуктов способствует потере фосфора. При жарке и запекании теряется порядка 40% макроэлемента, а при варке — от 50 до 70%. А сейчас мы перечислим некоторые продукты, лидирующие по содержанию фосфора в мг на 100 г:
- необработанные рисовые отруби — 1 680;
- очищенное конопляное семя — 1 650;
- жареные семечки подсолнуха — 1 160;
- горчичный порошок — 830;
- какао-порошок — 740;
- сыр пармезан — 700;
- сыр моцарелла — 550;
- сушеный укроп — 540;
- запеченный карп — 530;
- жареная говяжья печень — 500.

Можно отметить, что значимое количество фосфора содержится не только в сырах, но и других молочных продуктах. Кроме того, им богаты хлебобулочные изделия и сладкая выпечка. Некоторое количество макроэлемента наш организм восполняет из курицы, свинины, говядины, яичной и пшеничной лапши, яиц и свежих овощей.
Суточная норма потребления фосфора для детей и взрослых
Суточные нормы потребления фосфора зависят от возраста человека. Поскольку бо́льшая его часть содержится в костях и зубах, потребность в макроэлементе увеличивается в периоды активного роста организма. При этом беременные и кормящие женщины не испытывают повышенной потребности в фосфоре, так как под воздействием гормонов их кишечник высасывает фосфор гораздо активнее, чем в обычном состоянии. Ниже мы приводим рекомендуемые суточные нормы фосфора, рассчитанные для здоровых людей разных возрастных групп (в мг):
- до 6 месяцев — 100;
- 7 – 12 месяцев — 275;
- 1 – 3 года — 460;
- 4 – 8 лет — 500;
- 9 – 18 лет — 1 250;
- От 19 лет — 700.
Интересно, что, в отличие от кальция, потребность в котором увеличивается в зрелом возрасте, норма фосфора остается стабильной после 19 лет. Дело в том, что после окончания роста костей организму хватает того фосфора, который почки возвращают обратно в кровь. Кроме того, фосфор обладает более высокой биодоступностью, чем кальций, и в значительных количествах содержится в клетках.
Дефицит фосфора: причины, симптомы и последствия
Дефицит фосфора, также известный как гипофосфатемия, — это крайне редкое состояние, достичь которого практически невозможно в результате низкого потребления с пищей. Исключениями являются тяжелые проблемы вроде анорексии или голода, однако в этих случаях организму не хватает всех питательных веществ. Наиболее распространенными причинами гипофосфатемии являются нарушения всасываемости или усвояемости, вызванные следующими факторами:
- дефицит витамина D;
- частый и бесконтрольный прием препаратов от изжоги;
- хронический алкоголизм;
- заболевания почек или щитовидной железы;
- генетические нарушения регуляции фосфатов.
Симптомы дефицита фосфора неспецифичны, то есть могут свидетельствовать и о других проблемах в организме. На ранних этапах нехватка АТФ провоцирует постоянную усталость и мышечную слабость. В попытках сэкономить энергию организм замедляет пищеварение, что сопровождается потерей аппетита. Со временем начинаются боли в костях и суставах, эмаль ослабляется, и зубы становятся хрупкими. При критическом дефиците организм теряет способность синтезировать новые цепочки ДНК, что блокирует деление клеток и обновление тканей.

Избыток фосфора: риски и осложнения
Одной из серьезных проблем современной продовольственной безопасности являются фосфатные пищевые добавки: регуляторы кислотности, стабилизаторы, разрыхлители и эмульгаторы. Они содержатся во многих продуктах питания: газировке, колбасах, плавленом сыре и выпечке, — провоцируя гиперфосфатемию, или избыток фосфора. В здоровом организме нормальным соотношением кальция и фосфора является 2:1. Когда уровень фосфатов в крови резко поднимается, организм стремится восстановить баланс и забирает кальций из костей, где хранится 99% этого макроэлемента.
Таким образом, постоянное избыточное потребление фосфора может привести к дефициту кальция. Это приводит к нарушению структуры и снижению прочности костей, то есть развитию остеопороза. Кроме того, вытянутый из твердых тканей кальций связывается с фосфором в крови, образуя микрокристаллики — кальцинаты. Эти образования оседают на стенках сосудов, одновременно повышая их жесткость и ломкость. Кальцификация сосудов является распространенной причиной гипертонии и атеросклероза, а также повышает риск инфарктов и инсультов.
Лекарственные формы фосфора и правила приема
Когда речь заходит о фосфорсодержащих препаратах, важно понимать, что их ни в коем случае нельзя принимать без необходимости, а только после согласования с лечащим врачом. Как правило, пациентам назначают минеральные комплексы — фосфаты кальция или магния, — с целью предотвратить или нивелировать дефицитные состояния. Также больным часто прописывают фосфолипиды — органические соединения фосфора с жирами. Они являются частью комплексного лечения заболеваний печени, а также могут служить поддержкой для мозга и нервной системы.
Фосфор в спорте и при высоких нагрузках
Как мы уже знаем, для спортсменов и людей, испытывающих физические нагрузки, фосфор представляет особенную важность как неотъемлемая часть креатинфосфата, дающего дополнительную энергию. Также в спортивной медицине используют так называемые фосфатные буферы — растворы, содержащие калий или натрий. Они работают как химические нейтрализаторы, стабилизируя уровень кислотности клеток. Прием фосфатных буферов отодвигает порог усталости, позволяя выполнять упражнения дольше и эффективнее. Бегуны и пловцы принимают добавки с фосфором для повышения выносливости. Они повышают концентрацию 2,3-бифосфоглицериновой кислоты в эритроцитах, облегчая передачу кислорода от гемоглобина к тканям.

Взаимодействие фосфора с другими витаминами и минералами
Главными синергистами фосфора, то есть веществами, которые благотворно влияют на его усвоение, является кальций и витамин D. При этом важно соблюдать баланс — навредить организму может избыток не только фосфора, но и кальция, способствующего образованию нерастворимых солей. Без витамина D оба макроэлемента попросту не могут всасываться кишечником. Для правильной работы АТФ необходимо поддерживать нормальный уровень магния, ионы которого контролируют своевременное отщепление фосфатных групп.
Несмотря на совместную работу при энергетическом обмене, в кишечнике фосфор и магний являются антагонистами, то есть мешают усвоению друг друга при обильном одновременном потреблении. К такому же эффекту приводят продукты питания и биологически активные добавки с высоким содержанием железа, алюминия и цинка. При необходимости принимать фосфор с его антагонистами рекомендуется выдерживать промежуток между их употреблением не менее 2 – 3 часов.
Фосфор в вопросах и ответах
1. Что такое фосфор и зачем он нужен организму?
Фосфор — это макроэлемент, который является структурной частью костей и зубов, участвует в энергетическом обмене и связывает цепочки молекул ДНК.
2. Кто и когда открыл фосфор?
Фосфор в 1669 году открыл немецкий алхимик Хенниг Бранд.
3. В каких продуктах питания содержится больше всего фосфора?
Большое количество фосфора содержится в отрубях, семенах, молочных и мясных продуктах.
4. Сколько фосфора нужно человеку в день?
Здоровый человек в возрасте от 19 лет нуждается в 700 мг фосфора ежедневно.
5. Как фосфор влияет на прочность костей и зубов?
Фосфор входит в состав минерала гидроксиапатита, который является ключевым структурным компонентом костей и зубов.

6. Как фосфор участвует в энергетическом обмене?
Фосфор является частью молекул аденозинтрифосфата, которые высвобождают энергию, разрывая связи с фосфатными группами.
7. Чем опасен дефицит фосфора?
Дефицит фосфора может привести к патологическим переломам, мышечной недостаточности и неврологическим сбоям.
8. Какие признаки нехватки фосфора у детей и взрослых?
О дефиците фосфора могут свидетельствовать ослабление костей, разрушение зубов, хроническая усталость и мышечная слабость.
9. Что происходит при избытке фосфора в организме?
При избытке фосфора в организме нарушается минеральный баланс, что приводит к вымыванию кальция из костей.
10. Как связаны фосфор и кальций?
Фосфор и кальций вместе образуют минерал гидроксиапатит, обеспечивающий прочность зубов и костей.
11. Нужен ли фосфор спортсменам и людям с высокой активностью?
Фосфор критически важен для спортсменов и активных людей, так как удовлетворяет их повышенные потребности в энергии и дает дополнительную выносливость.
12. Можно ли получить достаточное количество фосфора только из пищи?
Да, полноценное разнообразное питание обеспечивает суточные потребности в фосфоре.
13. В каких случаях назначают препараты с фосфором?
Препараты с фосфором назначают, когда уровень фосфатов в крови падает ниже нормы.
14. Как фосфор взаимодействует с витамином D и магнием?
Витамин D стимулирует всасывание фосфора в кишечнике, а магний играет важную роль при отделении фосфатных групп во время выработки энергии.
15. Есть ли противопоказания к приему добавок с фосфором?
Да, добавки с фосфором могут быть противопоказаны при заболеваниях почек и нарушениях обмена кальция. Кроме того, избыток этого макроэлемента представляет угрозу для здоровья.
***
Будучи токсичным веществом в чистом виде, окисленный фосфор является неотъемлемой частью функционирования живых организмов. Помимо обеспечения крепости костей и зубов, он каждую секунду обеспечивает нас энергией, а также поддерживает сохранность молекул ДНК. Однако важно помнить и об опасностях избыточного потребления фосфора, отдавая предпочтение здоровому сбалансированному питанию.
Автор текста Иван Стефанов
Изображение на обложке: Ai-generated








