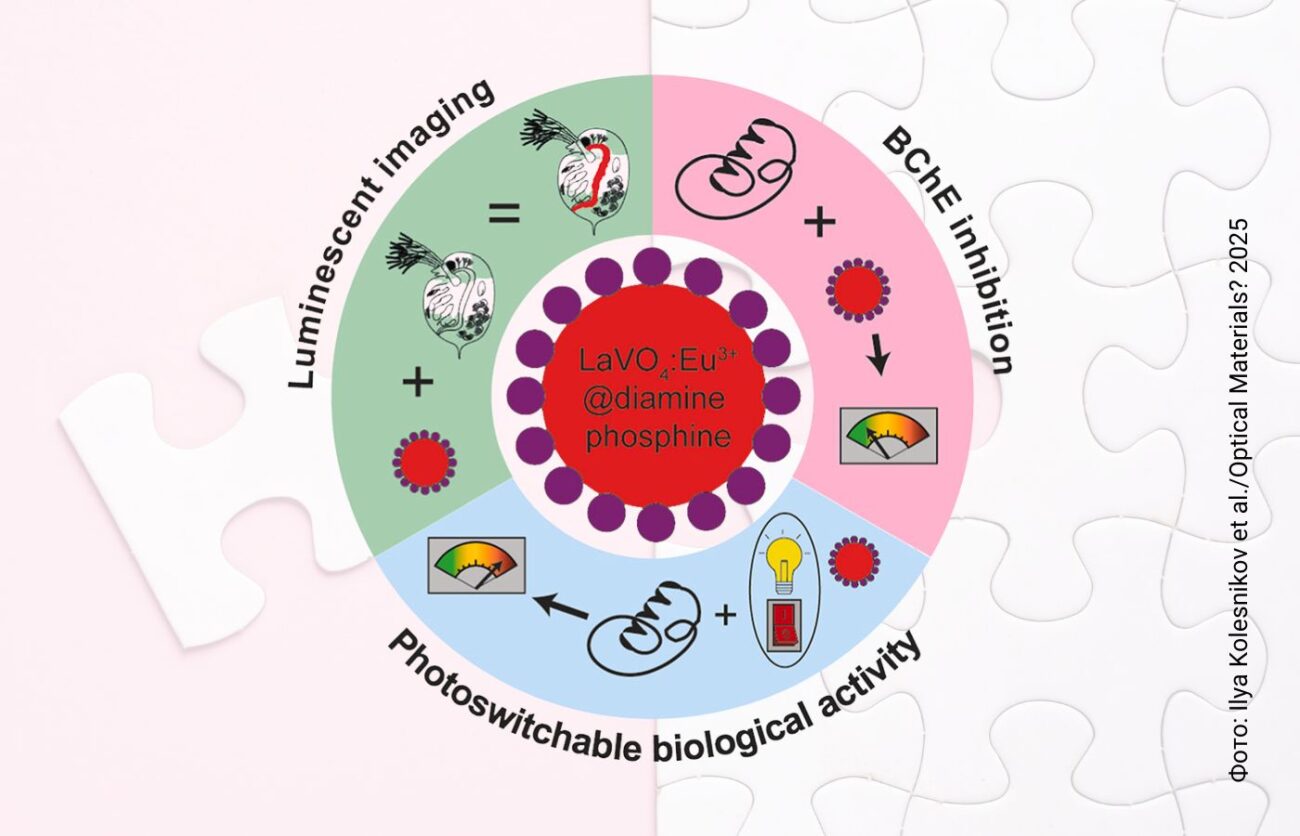
Специалисты Санкт-Петербургского государственного университета, Санкт-Петербургского Федерального исследовательского центра РАН и Санкт-Петербургского технологического университета разработали химическое соединение, активностью которого можно управлять с помощью лазера, а также отслеживать его местоположение в организме благодаря люминесценции. В перспективе синтезированное соединение найдёт применение в новых методиках таргетной терапии нейродегенеративных заболеваний: при активации оно способно блокировать фермент, повышенное содержание которого связано с развитием болезни Альцгеймера.
Исследование, поддержанное грантом РНФ, опубликовано в научном журнале Optical Materials.
Сегодня одной из наиболее перспективных альтернатив для обычной фармакологической терапии опасных заболеваний, например, болезни Альцгеймера, Хантингтона, Паркинсона, является адресная (таргетная) доставка лекарств. Такой подход обеспечивает транспортировку препаратов в заданную область организма, отдельный орган и даже клетку при помощи биотехнологических продуктов: наноразмерных капсул или частиц.
При этом, благодаря относительно высокой точности, таргетная доставка позволяет количественно уменьшить дозу лекарств, необходимых для лечения, а в случае применения токсичных препаратов — снизить общую нагрузку на организм. Однако пока уровень развития технологий не позволяет внедрить этот метод в широкую медицинскую практику. Поэтому научные коллективы по всему миру ведут разработки различных видов платформ и методов для доставки лекарств.
Петербургские ученые исследовали способность соединений блокировать бутирилхолинэстеразу — фермент, повышенное содержание которого связано с развитием болезни Альцгеймера у человека. Они показали, что новые наноматериалы превосходят аналоги по эффективности блокирования бутирилхолинэстеразы в два раза. Все оптические исследования наноматериалов, включая исследования в организмах рачков, проводились в Санкт-Петербургском государственном университете совместно с биологами из НИЦЭБ РАН — СПб ФИЦ РАН. Изучение возможности детектирования соединений проходило на инвертированном флуоресцентном микроскопе.
«Существующие фармакологические агенты часто сталкиваются с проблемами растворимости в воде и отслеживания в реальном времени в биологических объектах. Наш гибрид объединяет функции визуализации и фотопереключаемой терапии в единой платформе и, при этом является водорастворимым. Поэтому данная работа открывает новые возможности для фармакологии, предлагая надежную стратегию для создания направляемой визуализацией светочувствительной терапии нейродегенеративных заболеваний с высокой точностью и эффективностью», — отметила руководитель гранта РНФ, профессор кафедры лазерной химии и лазерного материаловедения СПбГУ Алина Маньшина.
Отсутствие токсичности и возможность локализации наноматериалов внутри организма при помощи люминесценции была показана на примере рачков (вид Daphnia magna Str.). Эти эксперименты продемонстрировали хорошую биосовместимость и адресное накопление в пищеварительной системе.
«Нашей команде удалось синтезировать биоактивный наноматериал, свойства которого можно запускать с помощью лазера, при этом способность к люминесценции позволяет установить его локализацию в организме. Кроме того, это первое подобное соединение, которое хорошо растворяется в воде. Последнее обстоятельство имеет большое значение для создания функциональных материалов для биомедицинских применений, открывая новые возможности в таргетной терапии», — рассказала старший научный сотрудник Лаборатории натурных эколого-химических исследований НИЦЭБ РАН — СПб ФИЦ РАН Анастасия Егорова.
Источник: РНФ
Изображение: наука.рф