Старение долго считалось неумолимой программой, встроенной в каждую клетку нашего тела — тихим таймером, который отсчитывает годы до их неизбежного угасания. Но что, если эта программа не так уж жестко зашита в нас и ее можно перенастроить? Новые открытия в генетике старения заставляют ученых всерьез задуматься: может ли человек продлить молодость дальше привычных границ?
Часики внутри нас и правда тикают
Старение — не просто постепенный износ организма, а четко прописанная программа, встроенная в каждую живую клетку. С момента рождения организма в ней запускается своеобразный биологический таймер, который медленно меняет его работу, накапливает сбои и в итоге приводит к естественному финалу. Снаружи это выглядит как течение времени, но внутри все управляется удивительно точными молекулярными механизмами.
Но если программа одна, почему же она «работает» с такой разной скоростью? Почему одни животные живут десятилетиями, другие — считанные месяцы? Почему такой разной бывает продолжительность жизни людей даже в схожих условиях?
На продолжительность жизни влияет несколько ключевых факторов.
- Защита от повреждений. Клетки постоянно сталкиваются со свободными радикалами и другими стрессами. Долгоживущие виды научились лучше чинить ДНК и эффективнее тушить такие «клеточные пожары».
- Особые гены. Иногда природа «выдает» видам полезные мутации, которые замедляют старение. Эти генетические настройки работают как улучшенный режим обслуживания организма.
- Удачное совпадение факторов. У людей долгожители чаще всего имеют удачный набор генов, спокойный метаболизм, низкий уровень воспаления.
На самом деле пределы жизни более гибкие, чем кажется. В природе есть настоящие чемпионы по долгожительству, например, гренландские киты, достигающие 200 лет, моллюски Arctica islandica, живущие до 500 лет.
У людей таких рекордов меньше, но они все же впечатляют. Самой долго жившей, документально подтвержденной персоной остается Жанна Кальман (1875-1997) из Франции, прожившая 122 года. Среди нынешних долгожителей — британка Этель Катерхем, которой 25 августа прошлого года исполнилось 116 лет. А число людей, преодолевших рубеж в 110 лет, в мире приближается к 150, так что, возможно, наш биологический предел еще далеко не достигнут.

На острие времени: как клетки решают, когда стареть
Чтобы понять, почему наш клеточный «таймер» вообще тикает, нужно опуститься на еще более глубокий уровень — туда, где хранятся инструкции жизни — хромосомы. На концах каждой хромосомы есть участок, который работает как предохранитель, не позволяющий генетическому материалу повреждаться при каждом делении клетки. Эти маленькие структуры называются теломеры и играют ключевую роль в том, как быстро стареет наш организм.
Они подобны пластиковым наконечникам на шнурках: пока они целы, шнурок служит долго, но когда начинают изнашиваться — расплетается. Каждый раз, когда клетка делится, ее теломеры становятся чуть короче. В какой-то момент защита исчезает, и клетка получает четкий биологический сигнал: продолжать делиться опасно. Это и есть один из фундаментальных механизмов старения — счетчик, который неумолимо отсчитывает наши клеточные «циклы».
Когда теломеры достигают критической длины, клетка выбирает одну из двух стратегий. Первая — апоптоз, аккуратное самоуничтожение. Это запрограммированный, почти идеальный процесс, в котором клетка «уходит» без вреда для окружающих тканей, как будто осознавая, что ее время пришло. Вторая — клеточная сенесценция. В этом состоянии клетка не умирает, но прекращает делиться и начинает функционировать словно пожилой работник, который перестал быть продуктивным, но по каким-то причинам остался в офисе. Сенесцентные клетки выделяют воспалительные молекулы, нарушая работу окружающих тканей и ускоряя общее старение организма.
Однако природа предусмотрела и противоположные механизмы — своеобразные «гены долголетия». Среди них особенно выделяются сиртуины, mTOR и FOXO.
Сиртуины работают как молекулярные хранители порядка: они регулируют восстановление ДНК, поддерживают метаболизм и помогают клеткам справляться со стрессом. Активность этих белков напрямую связана с продолжительностью жизни у многих организмов, от дрожжей до млекопитающих.
mTOR —, наоборот, клеточный «менеджер роста». Когда он активен, организм направляет ресурсы на рост и синтез, но в ущерб долгосрочному сохранению. Снижение активности mTOR, как показывают исследования, переключает организм в режим экономии и ремонта, продлевая клеточный срок службы.
FOXO-гены — своеобразные «директора по выживанию». Они активируются в условиях стресса и заставляют клетку переходить в режим восстановления, усиливая защиту от повреждений и повышая устойчивость к возрастным изменениям.
Все эти механизмы — от теломерного счетчика до генов долголетия — работают в тесной связке. Именно в этом переплетении сигналов, решений и биохимических путей скрывается ответ на главный вопрос: можно ли переписать программу старения и продлить жизнь дальше природного сценария?
Эксперименты, которые впечатляют
Если на первый взгляд непосвященного биологические механизмы старения кажутся абстракцией, то исследования последних лет превращают их в осязаемую реальность, которой можно управлять. Эксперименты ученых все чаще показывают: вмешиваться в клеточные программы можно и иногда это работает удивительно хорошо.
Одним из самых ярких примеров стали исследования на мышах с искусственно удлиненными теломерами. В результате такие мыши оказались заметно стройнее и здоровее своих обычных сородичей. Удлиненные теломеры не только улучшили обмен веществ, но и продлили жизнь мышей: средняя продолжительность увеличилась примерно на 13%, а максимальная — на 8%. При этом риск рака не вырос, напротив, опухоли у этих мышей встречались вдвое реже. Это стало первым убедительным доказательством того, что манипуляции с теломерами — путь к реальному продлению жизни.
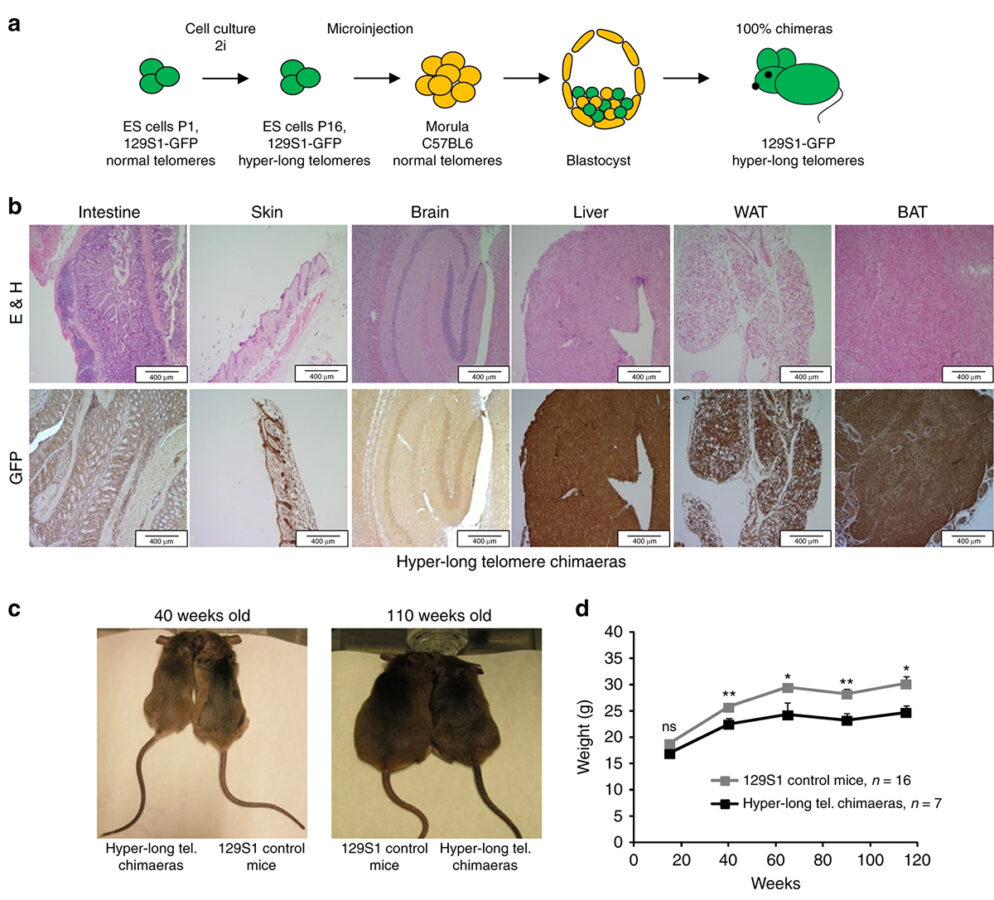
В 2022 году в журнале Nature описали эксперимент на мышах, в котором кратковременный прием рапамицина в ранней взрослой жизни надолго активировал защитные механизмы организма. Даже спустя месяцы после отмены препарата у подопытных организмов оставалась повышенная активность аутофагии — клеточного «ремонта», особенно в кишечнике. Таким образом, улучшились функции органов, снизились возрастные нарушения и заметно продлилась здоровая жизнь животных.
Эти эксперименты показывают: биологические часы можно не только замедлить, но и перенастроить. И хотя до практического применения этих методов на людях еще далеко, сама возможность вмешиваться в фундаментальные механизмы старения уже перестала быть мечтой.
Секреты долголетия: что предлагает современная наука
В поисках способов замедлить старение ученые исследуют не только гены и теломеры, но и молекулярные механизмы, связанные с энергией клеток. Одним из наиболее известных направлений в этой области стал поиск средств, защищающих митохондрии — «энергетические станции» клеток — от повреждений свободными радикалами. Среди российских разработок особое место занимает созданный в Московском государственном университете им. М.В. Ломоносова SkQ1 — «митохондриальный антиоксидант», который нацелен на нейтрализацию избыточных свободных радикалов прямо в митохондриях.
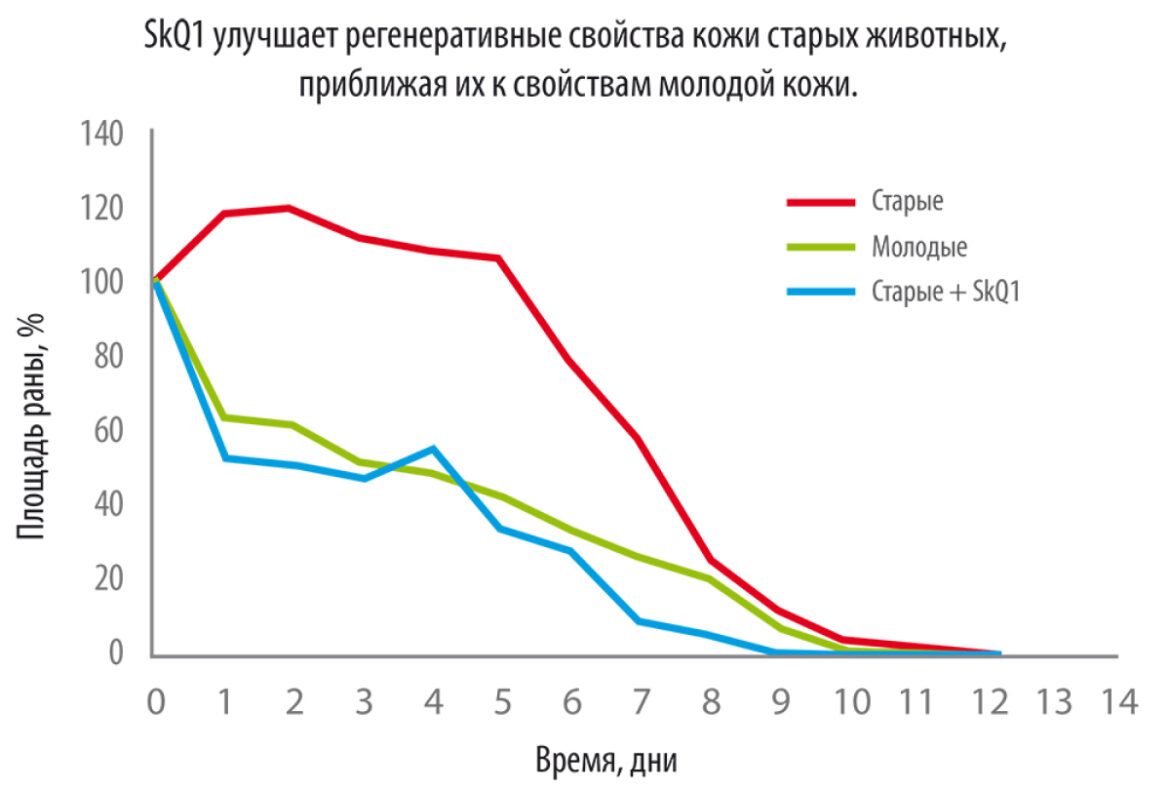
Эксперименты на мышах показали впечатляющие результаты: животные, получавшие SkQ1, жили в среднем на 15 % дольше и старели медленнее, по сравнению с контрольной группой.
На основе SkQ1 уже созданы препараты для человека: глазные капли Визомитин, мазь для кожи Экзомитин и косметические средства под брендом МитоВитан.
После обсуждения митохондриальных антиоксидантов стоит взглянуть на еще одно российское исследование, нацеленное на замедление старения —ученые из Волгоградского государственного медицинского университета разработали молекулу ВЛ-10.
ВЛ-10 обладает геропротекторными свойствами: она помогает предотвращать сахарный диабет, сердечно-сосудистые и нейродегенеративные заболевания, включая болезнь Альцгеймера.
Кроме того, препарат блокирует накопление метилглиоксаля — токсичного продукта метаболизма, который ускоряет старение. ВЛ-10 разрабатывается как биодобавка и планируется к выводу на рынок в рамках национальных проектов по продлению активной жизни и сохранению здоровья.
В числе ключевых российских инициатив в области исследования старения выделяется проект RUSS-AGE, направленный на создание «калькулятора биологического возраста» для населения России. Ученые собирают биоматериалы: кровь, плазму, ликвор и другие образцы от добровольцев разных возрастов и анализируют их по множеству показателей, включая эпигенетические метки и молекулярные признаки старения.

Помимо оценки биологического возраста, в рамках RUSS-AGE исследуются клеточные механизмы старения и ведется поиск геропротекторов — веществ, способных замедлять процессы старения, восстанавливать поврежденные ткани и поддерживать регенерацию органов. Этот проект интегрирован в национальные программы по сохранению здоровья и продлению активной жизни, открывая новые возможности для персонализированной медицины.
Таким образом, методы, позволяющие измерять «биологический возраст» и отслеживать клеточные «часы», становятся основой персонального подхода к замедлению старения. Если удастся точно определять возраст организма и корректировать эти показатели, то это может помочь предотвращать возрастные болезни и замедлять старение.
Тонкая грань между молодостью и опасностью
То, что в лаборатории выглядит как путь к замедлению старения, в человеческом организме может оказаться куда менее безопасным. Клеточные программы — теломеры, апоптоз, сенесценция — существуют не просто так. Это не «ошибки эволюции», а механизмы защиты. И вмешиваясь в них, мы неизбежно рискуем нарушить хрупкий баланс, который сохраняет организм здоровым.
Одно из самых серьезных последствий попыток «обмануть» клеточную смерть — риск развития рака. Заставляя стареющие клетки продолжать делиться или восстанавливать теломеры сверх естественной нормы, мы одновременно снимаем ограничения, которые природа поставила на бесконтрольный рост. Ведь опухолевые клетки — это те же наши клетки, только утратившие тормоза. Удлинение теломер, подавление апоптоза, отключение сенесценции могут подарить клетке вторую молодость, но вместе с тем и опасную свободу.

Кроме того, вмешательство в процессы старения может привести к нестабильности генома. Когда поврежденные клетки перестают «уходить» через апоптоз, они продолжают жить и копить ошибки — мутации, нарушения структуры ДНК. Со временем это не только снижает качество работы тканей, но и повышает вероятность образования опухолей или других тяжелых заболеваний.
Поэтому долголетие — это не просто стремление замедлить старение. Это поиск баланса: как сохранить молодость клеток, не лишая организм защитных механизмов, продлить срок службы тканей, не открывая двери для болезней.
Ученые больше озабочены не тем, как «отключить старение», а скорее тем, как сделать его более безопасным. Задача будущей медицины — не бессмертие любой ценой, а гармония между продолжительностью жизни и ее качеством.
Реальное будущее долголетия
Если заглянуть на 10-20 лет вперед, картина выглядит не фантастической, а вполне практичной. Нас ждут не «таблетки бессмертия», а более точные, персонализированные решения: лекарства, подобранные под наш геном и метаболический профиль; клеточные терапии, способные восстанавливать поврежденные ткани; аккуратные генные вмешательства, которые будут корректировать нарушения, не затрагивая при этом фундаментальные основы нашего биологического устройства, например ДНК.
Методы диагностики станут гораздо глубже: эпигенетические «часы» покажут реальный биологический возраст, а врач сможет отслеживать, как на него влияют образ жизни, питание и экспериментальные геропротекторы. Старение перестанет быть темной зоной биологии, оно станет измеримым и управляемым процессом.
Но важно понимать: наука движется не к волшебному эликсиру, который одним глотком вернет молодость, а к системному пониманию старения. И именно эта осторожность и есть фундамент будущих прорывов.
Автор текста Анастасия Будаева
Изображение на обложке: Freepik