Ученые разработали новый тип флуорогенного генетически кодируемого сенсора пероксида водорода — важной молекулы окислительного стресса и клеточного сигналинга. Сенсор HyPerFLEX позволяет отслеживать, где и когда в живых клетках появляются и действуют молекулы пероксида водорода на уровне клеточных компартментов (в ядре, эндоплазматическом ретикулуме, матриксе митохондрий, цитозоле). В отличие от существующих сенсоров, HyPerFLEX не требует кислорода для созревания флуорогена, что позволяет использовать его в условиях длительной гипоксии или в анаэробных организмах. Кроме того, биосенсор способен менять цвет свечения — от зеленого до красного — в зависимости от задач эксперимента. Такой подход открывает возможность с высокой точностью наблюдать за химическими реакциями внутри клеток. Полученный биосенсор позволит выявить роль пероксида водорода в разнообразных клеточных процессах и поможет в поиске новых способов диагностики и лечения заболеваний, в том числе нейродегенеративных.
Результаты исследования, поддержанного грантом Российского научного фонда (РНФ), опубликованы в журнале Nature Chemical Biology.
Пероксид водорода (H₂O₂) — одна из важнейших активных форм кислорода в организме. При очень малом уровне H₂O₂ запускает разнообразные клеточные сигнальные процессы, окисляя определенные белки и меняя их активность. Известно, что, будучи вторичным мессенджером — своеобразным «химическим посыльным» внутри клетки, — пероксид водорода меняет активность белков-регуляторов экспрессии генов (транскрипционных факторов) NF-κB, HIF, p53, FOXO. Эти белки управляют дифференцировкой клеток, их делением, воспалением, иммунными реакциями, старением и образованием опухолей, а также реакцией на недостаток кислорода, стресс и программируемую гибель клеток (апоптоз).
При больших концентрациях пероксид водорода перестает действовать избирательно. Он неспецифически окисляет белки, жиры и другие молекулы, повреждая их и вызывая окислительный стресс. Считается, что именно окислительный стресс лежит в основе многих нейродегенеративных заболеваний. При этом отследить образование и движение пероксида водорода внутри клетки крайне сложно. Поэтому важно понимать, где, когда и как он образуется и распространяется.
Обычно для наблюдения за молекулами внутри клеток используют флуоресцентные, светящиеся, белковые сенсоры. Но они не работают без кислорода, что затрудняет изучение процессов в клетках при его недостатке или у микроорганизмов, живущих без воздуха. Поэтому ученые ищут новые способы создания биосенсоров, которые могли бы работать в любых условиях внутри клетки, для отслеживания локальных изменений концентрации веществ и наблюдения за клеточной сигнализацией в норме и при патологиях.
Ученые Российского национального исследовательского медицинского университета имени Н.И. Пирогова (Москва), Федерального центра мозга и нейротехнологий ФМБА России (Москва), Научно-исследовательского центра LIFT (Москва), Института биоорганической химии имени академиков М.М. Шемякина и Ю.А. Овчинникова РАН (Москва) и физического факультета Московского государственного университета имени М.В. Ломоносова (Москва) с коллегами из Бельгии создали принципиально новый тип биосенсора — флуорогенный сенсор HyPerFLEX. Его сенсорная часть состоит из чувствительного к пероксиду белка OxyR бактерии Neisseria meningitidis. Репортерная, или сигнальная, часть выполнена по новому принципу: вместо обычного флуоресцентного белка использован Y-FAST, бактериальный белок, который сам по себе не светится, но способен «включать» свечение маленьких синтетических молекул — флуорогенов.
Сами по себе флуорогены флуоресцируют очень слабо, но как только они присоединяются к Y-FAST, загораются ярким светом. В биосенсоре Y-FAST соединен с сенсорной частью так, что яркое свечение возникает, только когда OxyR реагирует с пероксидом водорода. Важно отметить, что у ученых появляется возможность использовать флуорогены разных цветов — от зеленого до дальнекрасного — в зависимости от цели эксперимента и комбинации с другими сенсорами. Гибкость спектральных возможностей сенсора подчеркивает его название — HyPer with FLEXible FLuorogen EXitation.
В экспериментах по сравнению с самым чувствительным сенсором линейки HyPer — HyPer7 — исследователи обнаружили, что HyPerFLEX может фиксировать еще меньшие количества пероксида водорода в цитоплазме (жидкой части клетки), ядре и митохондриях (энергетических «станциях» клетки). Это делает его более точным и чувствительным инструментом, чем предыдущие сенсоры.
Испытания in vitro на клеточных культурах и тканях животных показали, что HyPerFLEX обладает высокой чувствительностью и широким диапазоном ответа. Ученым удалось создать версии сенсора, которые можно поместить в разные части клетки: в ядро, цитоплазму, митохондрии, на мембраны эндоплазматического ретикулума (органеллы, участвующие в синтезе белков и липидов) и вдоль актиновых филаментов (структур, поддерживающих форму клетки и транспорт внутри нее). HyPerFLEX стал первым сенсором, который позволяет наблюдать пероксид водорода даже в люмене эндоплазматического ретикулума — внутреннем пространстве органеллы, где окислительные процессы особенно сильны.
HyPerFLEX можно использовать для мультифотонной микроскопии, что позволяет наблюдать сигналы пероксида водорода глубоко внутри тканей — например, на срезах мозга мыши на глубине до 250 микрометров, что делает возможным изучение клеток прямо в живой ткани.
«Принцип создания флуорогенных биосенсоров, разработанный в исследовании, позволит конструировать новые сенсоры разнообразных метаболитов и сигнальных молекул для использования в живых клетках на уровне как отдельных клеточных компартментов и субкомпартментов, так и целой ткани или органа. В дальнейшем мы планируем расширить панель флуорогенов с тем, чтобы появилась возможность наблюдать за динамическими сигнальными и патологическими процессами в клетках с помощью микроскопии сверхвысокого разрешения, так как многие молекулярные события в клетке реализуются на нанометровой шкале. Кроме того, необходимо подобрать флуорогены, которые при системном введении в кровоток животных будут легко преодолевать гемато-энцефалический барьер, что позволит изучать редокс-метаболизм мозга в свободноподвижных животных», — рассказывает руководитель проекта Всеволод Белоусов, член-корреспондент РАН, директор Федерального центра мозга и нейротехнологий ФМБА России, заведующий лабораторией Синтетических нейротехнологий Пироговского Университета.
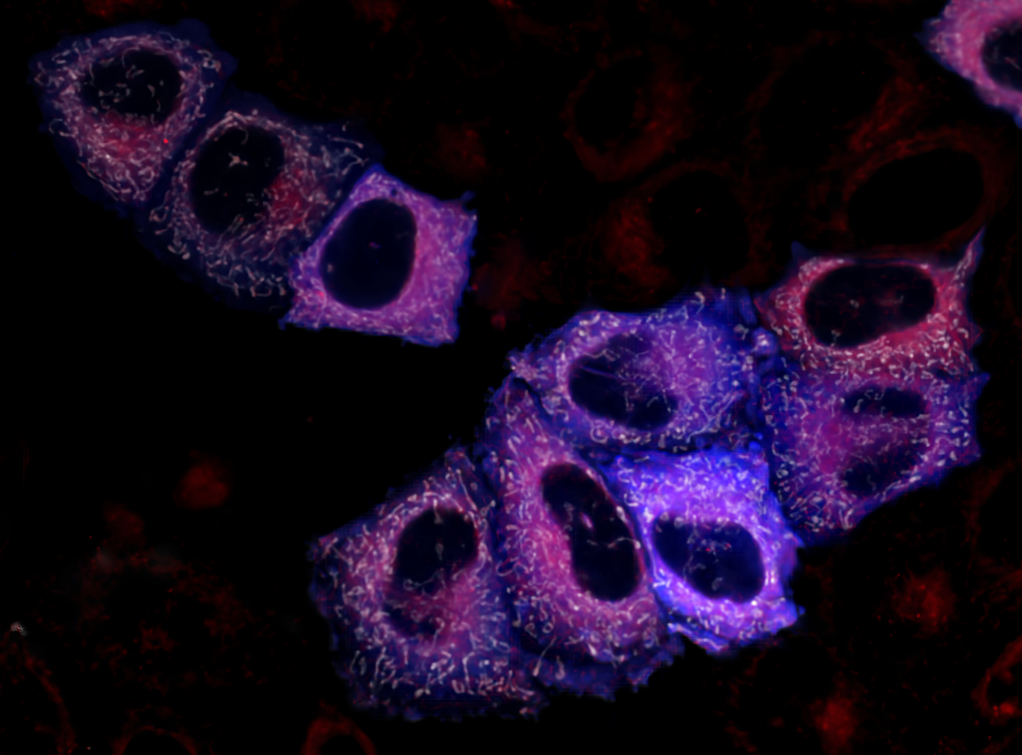
Изображение на обложке: Мультипараметрическая визуализация продукции пероксида водорода в люмене ЭПР клеток HeLa Kyoto хемогенетическим инструментом HyPerRed-DAO-ERlumen (красный) с одновременной детекцией его распространения в митохондрии сенсором mito-HyPerFLEX(3a) (белый), и цитозоль сенсором HyPer7-NES (синий). Псевдоцвета. Источник: Екатерина Потехина
Источник: РНФ