Исследования специалистов ЮФУ и Института неорганической химии им.
А. В. Николаева показали, что цитотоксическая активность изученных
комплексов меди в несколько раз превышает активность широко
используемых коммерческих противоопухолевых препаратов. Есть
вероятность, что в будущем полученные результаты внесут существенный
вклад в разработку новых противораковых лекарств.
Одна из важнейших задач бионеорганической и медицинской химии — это
получение новых лекарственных препаратов для диагностики и лечения
таких социально значимых болезней, как онкология. Сегодня в клинической
практике широко используются препараты на основе комплексов платины(II)
и платины(IV) (цисплатин, карбоплатин, недаплатин и др.). Но несмотря на
эффективность, они обладают недостатками, ограничивающими их
использование: токсичность, способность вызывать аллергические реакции,
снижение иммунитета и неизбирательность действия. Ученые уже сейчас
ищут новые препараты на основе соединений эндогенных металлов (кобальт,
медь, цинк, железо) с незначительными побочными эффектами и широким
спектром действия. Особое внимание уделяется комплексам меди, так как
она необходима для нормальной клеточной активности живого организма.
Коллектив кафедры физической и коллоидной химии им. проф. В.А. Когана
химического факультета ЮФУ совместно с учеными НИИ физики ЮФУ,
НИЦ «Курчатовский институт» и Института неорганической химии им. А. В.
Николаева СО РАН (г. Новосибирск) предположили, что синтез рядов бис-
гидразонов и комплексов меди на их основе позволит установить
взаимосвязь между структурой и противоопухолевой активностью
координационных соединений и, в конечном итоге, внесет существенный
вклад в понимание механизмов действия комплексов меди на раковые
клетки.
Более ранние исследования противоопухолевых свойств комплексов меди
показали, что их активность во многом определяется синергизмом свойств
металлоцентра и окружающих его органических молекул (лигандов). Так,
направленно изменяя природу заместителей а лиганде и их пространственное
расположение можно влиять на структуру и, как следствие, на
биологическую активность комплексов.
Несмотря на то, что открыто большое количество медьсодержащих
соединений с высокой цитотоксической активностью (некоторые из них
находятся на стадии доклинических и клинических испытаний), их
применение в качестве лекарственных препаратов пока представляется
преждевременным, так как во многих случаях нет данных о механизме
действия комплексов на раковые клетки и требуются дополнительные
биохимические исследования. В связи с этим, синтез и физико-химическое
исследование систематических рядов комплексных соединений меди – это
актуальная задача для изучения факторов, влияющих на противоопухолевые
свойства соединений и важнейший шаг в сторону получения надежных и
безопасных антираковых препаратов.
«Одним из подходов получения противоопухолевых веществ является синтез
комплексов на основе лигандов, обладающих биологически активными
свойствами. К таким системам относятся гидразоны моно- и
дикарбонильных соединений. Биологической активности гидразонов
посвящено множество работ, в которых обсуждаются их антивирусные,
противомикробные, фунгицидные, противоопухолевые и многие другие
свойства. В ряду гидразонов имеется ряд лекарственных средств
разнообразного действия – фурацилин, фтивазид, метисазон и другие.
Поэтому для реализации наших задач в качестве лигандных соединений
предполагается использовать бис-гетарилгидразоны, содержащие
пиримидиновый, фталазиновый, хинолиновый, бензимидазольный и другие
гетероциклы. По нашему мнению, такой выбор лигандов не только позволит
изучить влияние природы донорных атомов и гетероциклических
фрагментов на цитотоксическую активность бис-гидразонов и их медных
комплексов, но также сделает возможным получение взаимосвязи между
строением комплексов и их свойствами», – рассказала доцент кафедры
физической и коллоидной химии имени профессора В.А. Когана
химического факультета ЮФУ Юлия Туполова.
Таким образом, в своей научной работе ученые осуществили синтез серии
комплексов меди(II) на основе лиганда, содержащего активные
гетероциклические фрагменты – пиридин и хинолин. С помощью широкого
набора методов исследования была надежно установлена их структура.
Показано, что в зависимости от природы соли меди(II) образуются
комплексы различного состава и строения (рис. 1 и 2).
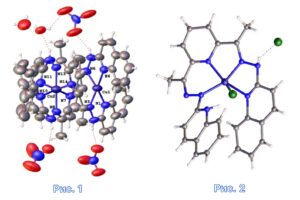
Биологические испытания синтезированных соединений против раковых
клеток Hep2 (карцинома гортани человека) и HepG2 (раковые клетки печени)
проводились in vitro (то есть в искусственных условиях, вне живого
организма) учеными в Институте неорганической химии им. А. В. Николаева
в г. Новосибирске.
Исследования показали, что все комплексы меди проявляют
цитотоксическую активность в несколько раз превышающую активность
широко используемых коммерческих противоопухолевых препаратов –
цисплатина и карбоплатина и открыли новые направления дизайна
перспективных комплексов, обладающих противораковой активностью. Для
более детального понимания взаимосвязи между строением изучаемых
соединений и их противоопухолевой активностью требуются дальнейшее
исследование систематических рядов бис-гидразонов и комплексов меди на
их основе.
Результаты исследования, поддержанного грантом Российского научного
фонда (РНФ) № 22-23-01161, опубликованы в издании Polyherdon.




Нет комментариев